干货| CTC PD-L1检测在临床上的应用(下)
上周我们介绍了 CTC PD-L1检测辅助黑色素瘤以及胃癌的预后评估,疗效评估以及受益人群筛选等等,但CTC PD-L1检测远不止在这两个癌种上辅助临床诊断,下面让我们再看几篇文章,对CTC PD-L1检测有个更深入的了解。
CTC PD-L1检测辅助肝癌预后评估与受益人群筛选
Paul Winograd等人[1]为探讨肝癌患者CTC上PD-L1表达的可行性和潜在意义,从87例肝癌患者(早期49例,局部晚期22例,转移性16例),7例肝硬化患者和8例健康对照的前瞻性队列中进行CTC的计数/表型分析,评估了CTC PD-L1的表达与免疫治疗的总体预后和治疗反应的关系。
结果发现,PD-L1+CTC在49例早期肝癌中检出4例(8.2%),但在22例局部进展期患者中检出12例(54.5%),在16例转移性肝癌患者中检出15例(93.8%),早期与局部进展期/转移性肝癌有较准确的鉴别(敏感性=71.1%,特异性=91.8%,受试者工作特征曲线下ROC面积=0.807;P<0.001)(图1、图2)。

图1
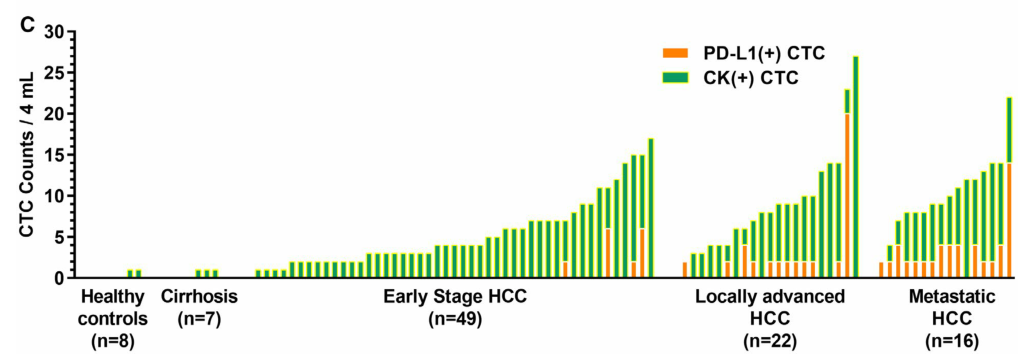
图2
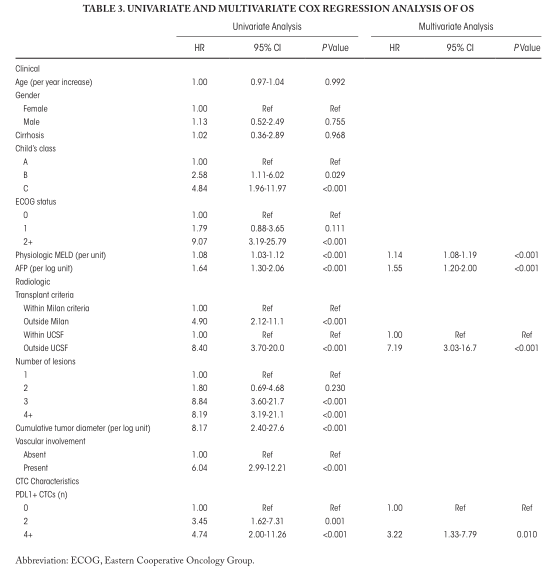
与阴性PD-L1+CTC的患者相比,PD-L1+CTC患者的总生存期(OS)显著降低(中位OS=14.0个月与未达,风险比[HR]=4.0,P=0.001)。在多变量Cox回归分析显示,即使在控制了终末期肝病模型评分(HR=1.14,P<0.001)、甲胎蛋白(AFP)(HR=1.55,P<0.001)和总体分期/肿瘤负担(HR=7.19,P<0.001)之后,PD-L1+CTC仍然是OS的独立预测因子(HR=3.22P=0.010)(图3、表1)。

图3
表1
在接受检查点抑制剂治疗的10名患者中,所有有反应的患者都有PD-L1+CTCs,而所有没有PD-L1+CTCs的患者治疗失败(图4)。但只有10名患者中的一小部分正在接受免疫治疗,这限制了我们对PD-L1+CTCs作为治疗反应的预测生物标志物的有效性得出明确结论。
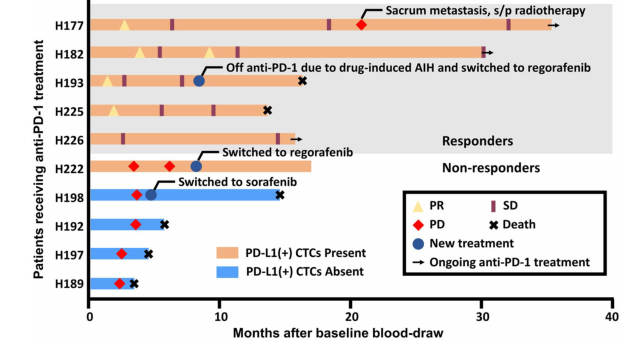
图4
研究表明,PD-L1+CTC主要发现于晚期HCC,在控制了终末期肝病模型、甲胎蛋白和肿瘤分期后,PD-L1+CTC独立预测OS。在接受抗PD-1治疗的肝癌患者中,PD-L1+CTCs的存在和良好的治疗反应有很强的相关性。在更大的队列中进行前瞻性验证将更好地确定PD-L1+CTCs作为肝癌预后和预测性生物标志物的实用性。
CTC PD-L1检测辅助消化道癌预后评估与动态监测
Chunyan Yue等人[2]为评估循环肿瘤细胞(CTCs)上PD-L1的表达能否作为一种替代的生物标志物。招募35名不同晚期胃肠道肿瘤患者参加了PD-1抑制剂IBI308的1期试验,并分析CTC计数和PD-L1表达水平。
结果显示,在IBI308治疗前,97%(34/35)的患者有CTC。74%(26/35)有PD-L1阳性CTCs,60%(21/35)至少有一个PD-L1高CTCs。92%的疾病控制(DC)患者(11/12)和65%的疾病进展(PD)患者(15/23)在基线时显示为PD-L1阳性CTC。我们特别检查了PD-L1高CTC的分布,发现21例患者存在这种情况。在无PD-L1高CTCs的患者中,只有14%(2/14)的患者对IBI308有反应,而48%的PD-L1高CTCs患者(10/21)对IBI308有反应(图5)。我们观察了Pd-L1高CTC的比例分布,并定义了20%为阈值。

图5
在30例可供二次采血的患者中,73%(8/11)DC患者和11%(2/19)PD患者总CTC下降。在PD-L1表达分析中,55%(6/11)的DC患者PD-L1阳性细胞总数下降,95%(18/19)的PD患者升高(
,P<0.002),而PD-L1高CTC计数分析中,64%(7/11)DC患者降低,84%(16/19)PD患者升高或保持不变(16/19)(P<0.007)。这些结果表明,总CTC、PD-L1阳性CTC和PD-L1高CTC的计数变化与疾病转归有很好的相关性(图6)。

图6
以20%为阈值,高于阈值的PD-L1高CTC患者较低于阈值的患者有明显更长的PFS(P=0.002),中位PFS为4.27 vs 2.07个月(图7)。

图7
研究表明,PD-L1高 CTCs在基线水平的丰度对PFS有预测意义,PD-L1高CTC水平可作为筛选PD-1/PD-L1阻断治疗患者的预测指标,CTC表达的动态变化可更早地提示治疗反应。
CTC PD-L1检测辅助乳腺癌预后评估
William Jacot等人[3]为探究CTC上PD-L1表达的预后价值。招募72例转移性乳腺癌(MBC)患者,检测PD-L1(+)-CTCs水平,并评估其临床病理相关性和预后价值。
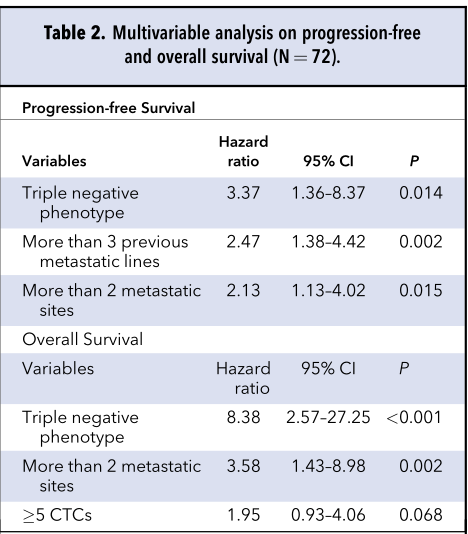
COX多变量分析显示,在单因素分析中,三重阴性(TN)表型、HR/HER2状态、>3次转移治疗、>2个转移部位、PD-L1(+)-CTC计数与PFS显著相关,而组织PD-L1表达与PFS无关;PR、TN表型、>2个转移部位和≥10基线CTC计数与OS显著相关。在多变量分析中,TN表型、>3次转移治疗和>2个转移部位是PFS的独立变量;TN表型和>2个转移部位是OS的独立变量(表2,表3)。
表2

表3
以PD-L1(+)-CTC计数1为阈值,PD-L1(+)-CTC≥1的转移性乳腺癌患者 PFS显著低于PD-L1(+)-CTC=0的患者(P=0.03),PD-L1(+)-CTC与OS之间则无显著相关性(图8)。

图8
结论:PD-L1(+)CTCs与MBC的存活率相关,组织PD-L1与MBC存活率无关。重新评估抗PD-1/PD-L1治疗下肿瘤组织和CTC的PD-L1表达的作用是有必要的,可以评估MBC患者治疗策略和试验分层的预测价值和潜在作用。
除此之外,还有很多研究已经证实CTC PD-L1检测在不同癌种不同临床中的应用,CTC PD-L1检测的临床应用价值是不可估量的。但是CTC PD-L1检测还处于完善阶段,它作为PD-1/PD-L1免疫检查点抑制剂伴随诊断的工具还需要大量研究,充足的数据支持理论,这也是临床和科研发展的方向!
参考文献:
[1] Paul Winograd, Shuang Hou, Colin M,et, al. Court Hepatocellular Carcinoma–Circulating Tumor Cells Expressing PD‐L1 Are Prognostic and Potentially Associated With Response to Checkpoint Inhibitors[J]. Hepatology Communications, 2020.Aug.
[2] Yue C , Jiang Y , Li P , et al. Dynamic change of PD-L1 expression on circulating tumor cells in advanced solid tumor patients undergoing PD-1 blockade therapy[J]. Oncoimmunology, 2018:00-00.
[3] William J , Martine M , Caroline M , et al. Clinical Correlations of Programmed Cell Death Ligand 1 Status in Liquid and Standard Biopsies in Breast Cancer[J]. Clinical Chemistry2020,(8).
1.采用目前最先进的鲱鱼骨结构纳米微流控芯片专利技术,全自动化CTC扫描检测。
2. 采用EpCAM和CSV双抗体捕获,PanCK、CSV和PD-L1三种抗体检测,同时实现各种CTC特异性分型捕获计数及CTC PD-L1的检测。
3. 可用于辅助免疫治疗药物伴随诊断,免疫治疗、手术、放(化)疗及新辅助化疗的预后评估、疗效监测和疾病进展监测。
华得森微信小商店已经上线了,有需要的客户须遵循肿瘤科专业医生的指导在线下单。
识别下方程序码进入商店。

关于华得森
杭州华得森公司是国家高新技术企业、浙江省科技型企业、杭州市高新区高成长型“瞪羚企业”、杭州市科技型“雏鹰计划”重点支持企业。公司旗下“杭州华得森精准医学检验技术研发中心”被认证为浙江省级高新技术企业研究开发中心、杭州市级企业高新技术研究开发中心。
公司以“精准诊疗”为发展核心,以“液体活检”为技术导向,集研发、生产、技术服务为一体,专注于开发创新技术和检测分析仪器、诊断试剂产品,坚持“CTC检测分析一体化、CTC临床应用标准化、CTC伴随诊疗精准化”作为创新驱动发展的前进方向,志在成为中国CTC行业的领跑者和中国最好的液体活检公司,努力为人类健康产业的发展,带来突破和创新!