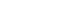液体活检新势能,CTC行业新标杆

华得森CytoSorter®CTC检测系统自2021年7月获国家药监局批准注册三类证以来,备受临床专家、业界人士广泛关注。华得森CytoSorter®系统获得的大规模的多中心临床研究成果,为CTC检测技术的标准化、系统化,临床应用的精准化、多样化树立了新的标杆。
CTC检测目前在头部三甲医院开展相对广泛,但缺少经过广泛验证的权威标准,CytoSorter®CTC检测系统的获证上市,各地市场反响强烈。自八月以来,包括西安、广州、上海等多家国内知名三甲医院已经完成了CytoSorter® 循环肿瘤细胞检测系统的正式进院。同时浙江、上海、江苏、山东、广东、陕西、山西、河北、安徽、福建等省市的多家头部医院已完成CytoSorter®循环肿瘤细胞检测系统的立项工作或入院前的产品性能验证工作;据不完全统计,华得森生物三类注册证颁布后新增订单销售金额已逾2亿元人民币。同时,拟启动多中心临床试验的CTC伴随诊断试剂产品已达5个拟推出用于临床咨询服务和临床研究的LDT达16个,将会极大的推动CTC技术的发展、拓展临床应用的空间。
CytoSorter®循环肿瘤细胞系统的获准上市,得到了众多临床专家的认可和赞誉,具有划时代的意义。正如专家审评会议上全国著名临床检验诊断学专家康熙雄教授所言:“CytoSorter®是一款CTC富集检测效率、临床符合率较高的技术平台,是一款既满足临床诊疗,又满足临床科研的技术平台。CytoSorter®的获证将极大推动CTC在肿瘤临床广泛应用和实验室常规化,必将为肿瘤临床诊疗变革做出突出贡献。”中山大学孙逸仙纪念医院检验科主任段朝辉教授也给予了较高的评价:“基于规范实验设计的CTC多中心临床研究,目前国内开展的不多,华得森走在行业的前面,打造出一个CTC检测的新标杆。”浙江大学医学院附属第二医院常务副院长黄健院长作为临床研究总负责人对华得森也给予了充分的认可:“华得森在乳腺癌、肺癌、前列腺癌、结直肠癌上的多中心临床研究数据,基本跟临床实际验证的数据一致,符合现阶段临床对于CTC辅助肿瘤精准诊疗的需求!”
时值2021即将结束,新的一年即将到来,华得森生物乃至循环肿瘤细胞这一热门赛道又将有怎样的表现呢?让我们拭目以待。
2021年7月,国家药监局批准CytoSorter®CTC检测系统为医疗器械三类注册证。