CTC检测在肿瘤免疫治疗临床诊疗中的应用
(1)CTC PD-L1表达检测辅助肿瘤免疫治疗伴随诊断
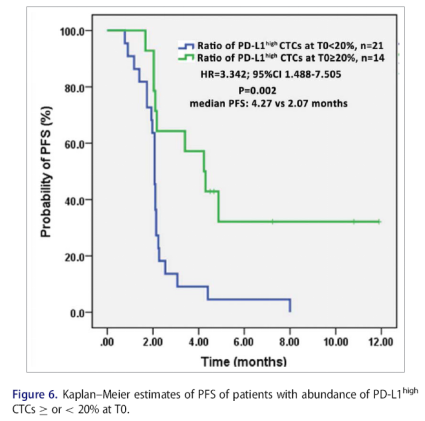
Yue C, Jiang Y, et al. Oncoimmunology. 2018 Mar 6;7(7):e1438111.
- 35名患有不同晚期胃肠道肿瘤的患者参加了PD-1抑制剂IBI308的1期试验。 PD-L1高表达患者的疾病控制(DC)率(48%)远高于其他患者(14%)。具有至少20%丰度的PD-L1高CTC的组具有甚至更高的DC率64%(9/14),其余的仅为14%的DC率(3/21)。
- 研究发现:基线时PD-L1高表达CTC可作为患者PD-1 / PD-L1免疫治疗的预测因子,并且测量CTC的动态变化可以早期指示治疗反应。
(2)CTC PD-L1表达检测辅助肿瘤免疫治疗疗效监测

Nicolazzo C, Raimondi C, et al. Sci Rep. 2016 Aug 24;6:31726
- 24名接受Nivolumab免疫治疗的IV期NSCLC患者进行CTC PD-L1检测。
- 在基线时,开始治疗后3个月和6个月评估表达PD-L1的CTC。在基线和治疗3个月时,发现CTC的存在和其表面上的PD-L1的表达与不良患者的结果相关。
- PD-L1阴性CTC患者均临床获益,而PD-L1(+)CTC患者均出现进展性疾病。这表明PD-L1(+)CTC的持续存在可能反映了治疗逃逸的机制。循环肿瘤细胞(CTC) PD-L1检测可以监控免疫治疗效果、评估预后。
(3)CTC PD-L1表达检测辅助肿瘤免疫治疗预后评估
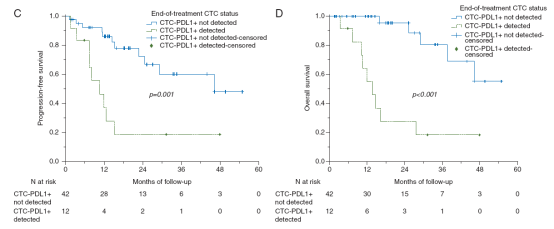
Strati A, Koutsodontis G, et al. Ann Oncol. 2017 Aug 1;28(8):1923-1933.
- 一项前瞻性队列研究中,113名局部晚期HNSCC患者,在诱导化疗2周(第6周)和同步放化疗结束后(周)评估CTC组分中的PD-L1表达。
- 在治疗结束时过表达PD-L1的CTC患者的无进展生存期(P = 0.001)和总生存期(P <0.001)较短。
- 多变量分析显示,治疗结束时PD-L1过表达是无进展生存期和总生存期的独立预后因素。
(4)CTC PD-L1表达检测辅助肿瘤免疫治疗疾病进展监测
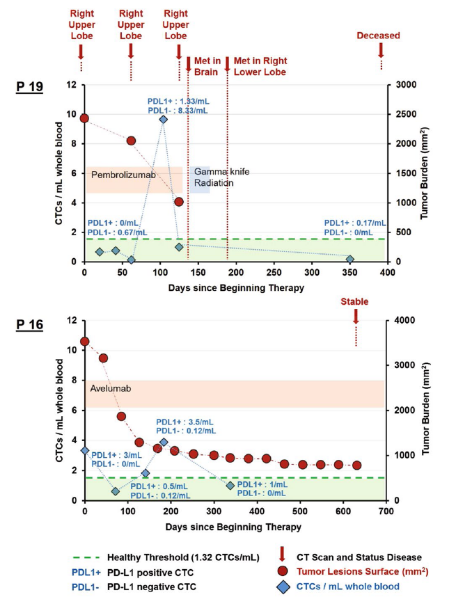
Dhar M, Wong J, et al. Sci Rep. 2018 Feb 7;8(1):2592.
- 转移性NSCLC患者免疫治疗前通过结合肿瘤组织IHC结果,与CTC 数量,CTC PD-L1 表达水平分析在后期治疗跟踪监测, PD-L1 阴性 CTC 比例较低的患者发生肿瘤转移最后死亡;PD-L1 阳性 CTC 比例较高的患者在用药后肿瘤病灶缩小,CTC数量减少,病情稳定。
(5)CTC PD-L1表达检测辅助肿瘤化疗临床诊断
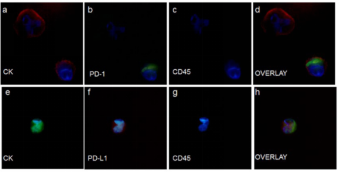
Kallergi G, Vetsika EK, et al. Ther Adv Med Oncol. 2018 Jan 15;10:1-11
- 化疗之前和之后从30名初治的IV期NSCLC患者中分离CTC。
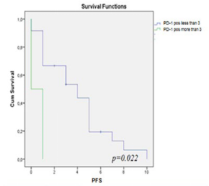
- 基线时≥3个PD-L1(+)CTC患者的中位无进展生存期(PFS)明显短于<3个PD-L1(+)CTC患者(p = 0.022)。
- 转移性NSCLC患者化疗治疗前存在高PD-L1(+)CTC数量与患者临床结果差相关。
(6)CTC PD-L1表达检测辅助肿瘤放疗临床诊断
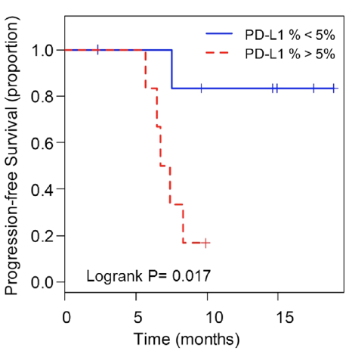
Wang Y, Kim TH, et al. Sci Rep. 2019 Jan 24;9(1):566
- 38个非转移性非小细胞肺癌患者外周血液样本,25个(69.4%)检测到PD-L1(+)CTC。在开始放射治疗后,PD-L1(+)CTC的比例显著增加(中位数0.7%对24.7%,P <0.01),表明肿瘤细胞中PD-L1对辐射的响应上调。
- 基线时PD-L1阳性(≥5%CTC阳性)患者的PFS较短。
- CTC PD-L1的动态变化可用于监测放射治疗期间治疗反应,评估预后。
2020年4月24日 15:33